Farbtheorie nach Witt
Witt postulierte eine Theorie, welche die Farbigkeit von organischen, konjugierten Farbstoffen erklärt. Nach Witt entsteht die Farbigkeit durch ein Zusammenspiel aus Chromophoren (in früheren Darstellungen Teil von Chromogenen) und Auxochromen.
Chromophore
Chromophore sind Grundstrukturen, welche delokalisierte Elektronen / konjugierte Doppelbindungen (zumindest im Organischen) enthalten.
Diese erfüllen die Grundanforderungen für Farbstoffe, wobei die Farbigkeit von dem Absorptionsbereich abhängt.
Insgesamt gilt: Je höher die Elektronendichte, desto stärker die Delokalisation, desto weniger Energie (größere Wellenlänge wird zur Anregung benötigt).
M-Effekt
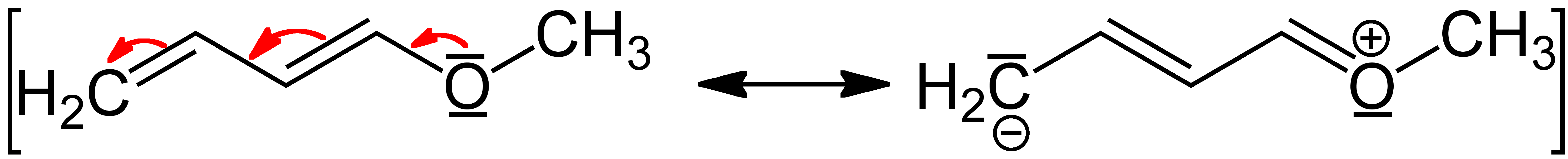
+M-Effekt
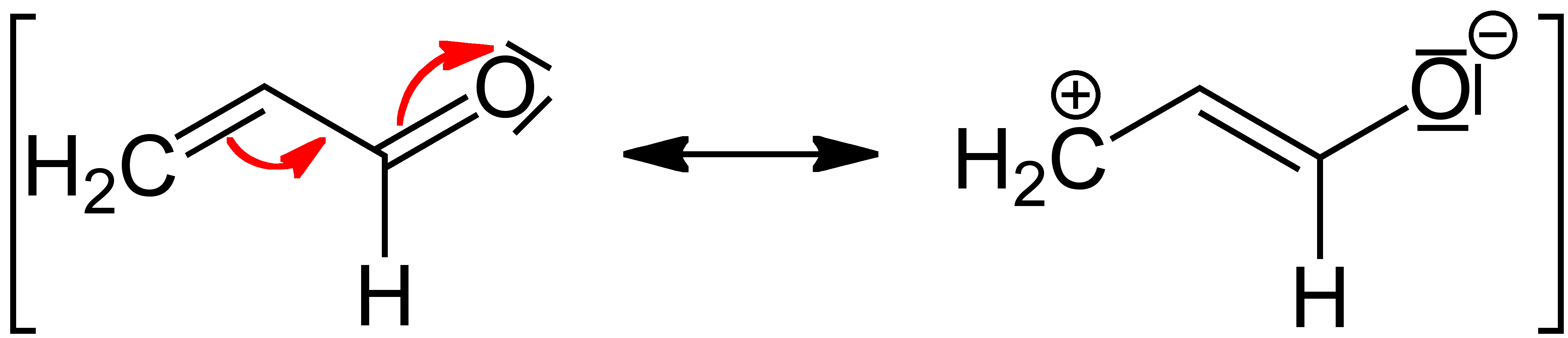
- M-Effekt
Auxochrome
Auxochrome sind Gruppen, die den Absorptionsbereich einer färbenden Gruppe (Chromophor) in das Längerwellige verschieben (Rotverschiebung). Dies nennt sich Farbvertiefung oder bathochromer Effekt. Die Verschiebung der Absorption geschieht meist durch einen +M-Effekt, welcher für höhere Elektronendichte im System sorgt. → kleinere Energiedifferenz zwischen höchstem mit Elektronen besetzten (HOMO) und dem niedrigsten unbesetzten (LUMO) Orbital → Rotverschiebung der Absorption
Liste von Auxochromen, mit zunehmender Farbvertiefung
-OCH3, -Halogen, -OH, -NHCOR, -NH2, -NHR, -NR2, -NHAr
Antiauxochrome
Antiauxochrome sind funktionelle Gruppen mit einem -M-Effekt. Beispiele: Carbonyl- oder Nitrogruppe (–NO2)
Wirkung in Verbindung mit Auxochromen
In Verbindung mit Auxochromen kommt zu einem Push and Pull Effekt auf Elektronen zwischen Auxochrom und Antiauxochrom, hierdurch wird die Bathochromie verstärkt.
Wirkung allein
→ wahrscheinlich als Hypsochrome
Hypsochrome
Diese funktionellen Substituenten besitzen einen -I-Effekt (elektronenziehend) und führen zu einer verschiebung des Absorptionsspektrums in einen kurzwelligen Bereich (Blauverschiebung der Absorption) (hypsochromer Effekt). (je nach Definition auch Antiauxochrome)
Hyperchromer Effekt
- mehr Absorption
- oft durch Auxochrome
Hypochromer Effekt
- weniger Absorption
Solvatochromie
- Beeinflussung der Absorption durch Lösungsmittel
- zum Beispiel beim Übergang von einem unpolaren zu einem polaren Lösungsmittel: Wasserstoffbrücken wirken stabilisierend → hypsochromer Effekt
Halochromie
- Farbvertiefung durch Salzbildung
- kleinere HOMO-LUMO Differenz bei Salzen (energetisch günstigere Mesomerie)
Sie möchten mir einen Kaffee spendieren?
Anmerkungen oder sonstige Ideen und Vorschläge können Sie gern per Mail an info@lernzettel.org bzw. fehler@lernzettel.org senden.