Wasserhärte – Bedeutung und Enthärtung
Die Wasserhärte ist ein Maß für die Konzentration an Calcium-Ionen und Magnesium-Ionen, welche in Grad deutscher Härte angegeben wird. 1 Grad deutscher Härte bedeutet hierbei, dass in 100 L Wasser ebenso viele Calcium-Ionen wie in einem Gramm Calciumoxid enthalten sind.
Beim Erhitzen von Wasser fällt Kalk (Calciumcarbonat ()) aus, da beim Erhitzen Calcium-Ionen mit im Wasser vorhandenen Hydrogencarbonat-Ionen reagieren:
Auch reagieren die Anionen von Seifen mit den Calcium-Ionen zu Kalkseifen, welche die volle Waschwirkung verhindern und sich bei Kleidung im Gewebe festsetzen.
Enthärtung
Um Wasser zu enthärten, müssen die Calcium- und Magnesium-Ionen aus dem Wasser entfernt werden.
Kationenaustausch
Eine Methode ist der Kationenaustausch durch beispielweise Natriumcarbonat.
Das Calciumcarbonat fällt aus.
Chemikalien zur Enthärtung von Wasser
Diese Chemikalien gehen starke Wechselwirkungen mit den Erdalkali-Kationen ein, sodass diese nicht mehr für störende Reaktionen zur Verfügung stehen. Sie werden nicht entfernt sondern eher ,,maskiert“.
Früher wurden Triphosphate genutzt, welche die für Härte sorgenden Kationen durch eine Komplexbildung binden. Allerdings gelangten diese durch die Abwässer in Seen und sorgten für Eutrophierung und werden heute deswegen zum Beispiel nicht mehr genutzt.
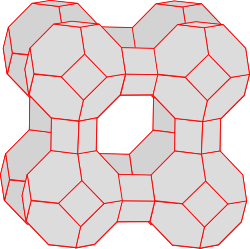
Heutzutage wird Zeolith A genutzt. In der Käfig-Struktur dieses Anions befinden sich Kationen, wobei bestimmte bevorzugt werden. So können abgegeben und aufgrund der ,,Bevorzugung“ gegen ausgetauscht werden.
Empfehlungen
Sie möchten mir einen Kaffee spendieren?
Anmerkungen oder sonstige Ideen und Vorschläge können Sie gern per Mail an info@lernzettel.org bzw. fehler@lernzettel.org senden.