Chemie → Kohlenhydrate →
Monosaccharide
Allgemein
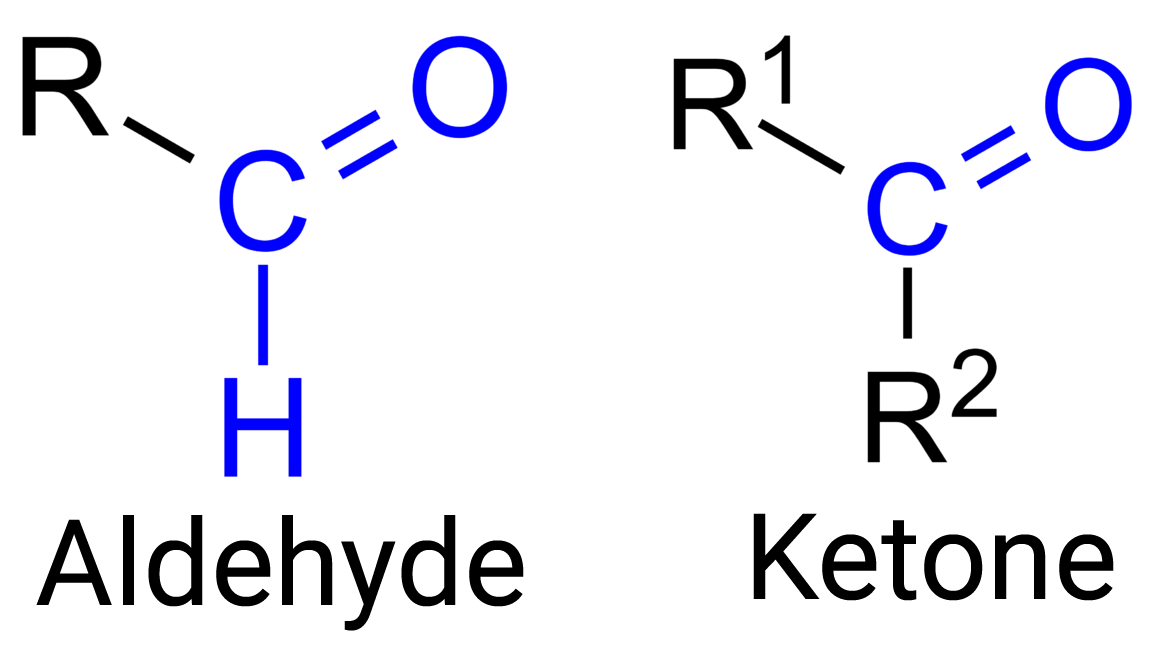
Monosaccharide sind eine Untergruppe der Kohlenhydrate. Sie bestehen aus einer Kohlenstoffkette, an welcher sich Hydroxy- und an der Spitze eine Aldehyd- / Ketogruppe befinden.
Fischer-Projektion
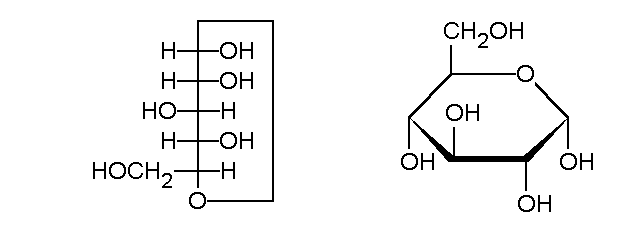
Die Monosaccharide können offenkettig vorliegen und werden dann in der Fischer Projektion dargestellt.
In dieser offenkettigen Form kommt es aufgrund der Asymmetrie (vier verschiedene Bindungspartner) der Kohlenstoffe 2-5 (bei den Hexosen) zu einer Isomerie. Da diese Bindungen nicht frei drehbar sind, gibt es zwei nicht deckungsgleiche Enantiomere jedes Monosaccharids. Es gibt einen Spiegelpartner, dies nennt man Chiralität. Die Hydroxygruppe am C5-Atom entscheidet ob die L oder D Form vorliegt. L steht für levus (links), D für Dextera (rechts). Es handelt sich um eine Spiegelbildisomerie.
Optische Aktivität
Saccharide sind optisch aktiv, die Polarisation des Lichts wird beim Durchstrahlen des Zuckers verändert. Falls Stoffe das Licht im Polarimeter nach rechts drehen, wird zu dem Namen ein + hinzugefügt, bei linksdrehenden Stoffen ein -. Die optische Aktivität kann mit der Isomerie zusammenhängen (interessant für den Contergan-Skandal), dies muss aber nicht der Fall sein. Ein Gemisch, in welchem sich die Drehungen gegenseitig aufheben heißt Racemat.
Haworth-Formel
Saccharide treten hauptsächlich in ihrer Ringform auf (nahezu 100%).
Die Glucose bildet eine Pyranose, also ein Sechseck. Über das Sauerstoffatom der Hydroxygruppe am C5 Atom kommt es zu einer Bindung. Die Aldehydgruppe wird zu einer Hydroxygruppe.
Quelle: Silvercat, Alpha-D-Glucose, CC BY-SA 3.0
Es bildet sich ein Halbacetal am C1 Atom (an ein Kohlenstoffatom sind sowohl eine OH (Hydroxygruppe) als auch eine OR (Alkoxygruppe) gebunden). Halbacetale können weiter zu Acetalen oxidiert werden.
Bei der Fructose sieht das Ganze ein wenig anders aus. Es handelt sich um eine Ketose, welche neben der Pyranose (Sechseck) auch eine Furanose (Fünfeck) bilden kann.
(Die L-Formen sind in der Grafik ausgelassen.)
Wie man sieht bildet sich entweder eine Bindung zwischen dem Sauerstoff der Hydroxygruppe am C5 oder C6 Atom mit dem am C2 Atom. Für die Gruppen an der Kohlenstoffkette gilt: FLOH - Fischer links, oben Haworth (auch bei der Glucose).
Anomere
Durch die Ringbildung wird auch das C2 Atom (Ketose) / C1 Atom (Aldose) asymmetrisch, es kommt zu zwei neuen Isomeren. Liegt die OH-Gruppe unten, handelt es sich um die α-Form, ist sie oben um die ß-Form. Da es einen ständigen Wechsel zwischen der offenkettigen und der ringförmigen Form gibt, kommt es zu einem Gleichgewicht von α-Form und ß-Form. Der Wechsel zwischen den Anomeren heißt Mutorotation. Im Polarimeter können die beiden Formen durch ihre unterschiedliche optische Aktivität unterschieden werden.
Konformere
Die Konformation ist die räumliche Anordnung von drehbaren Bindungen an Kohlenstoff Atomen. Konformere sind Moleküle mit gleicher Konfiguration aber unterschiedlicher Konformation.
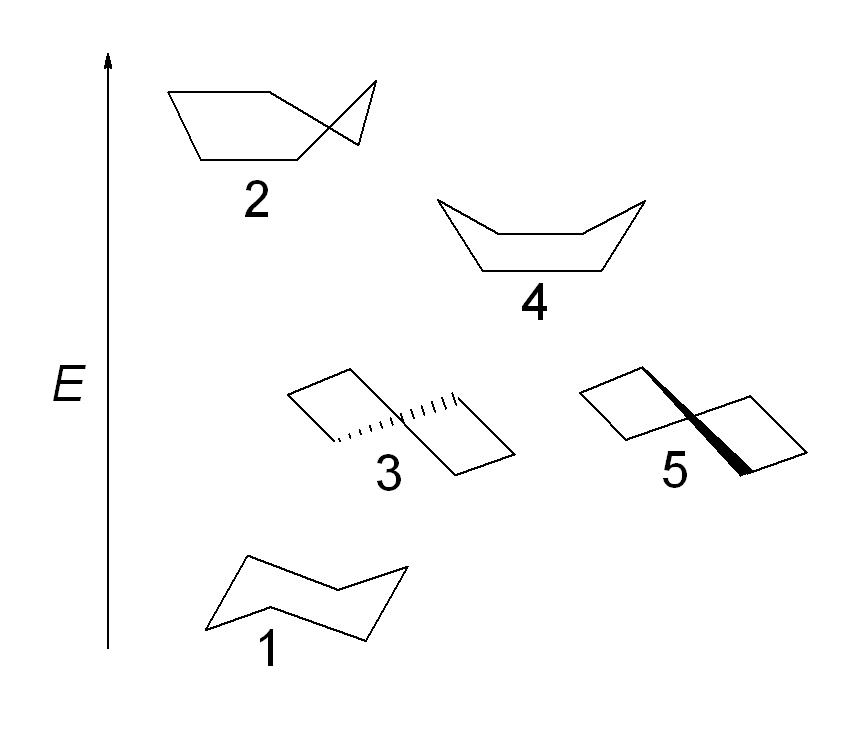
Sesselform
Wannenform
Bei der Wannenform (4) kommen sich Wasserstoff-Atome räumlich näher, die Energie steigt, die Stabilität sinkt.
Oxidierbarkeit
Da am C1 ein Halbacetal vorliegt, ist eine Kettenöffnung und Oxidation möglich. Bei Ketosen kommt es zu einer zusätzlichen Umlagerung (siehe Auswertung Versuche).
Drehbarkeit
Monosaccharide können gedreht werden. Bei einer Drehung um 180° nach links / rechts werden durch die räumliche Anordnung (vorne / hinten) auch die Substituenten eines C-Atoms einmal gedreht. Hydroxygruppen, die vorher nach oben zeigten, zeigen jetzt nach unten. Bei einer Drehung nach unten gibt es diesen Tausch auch.
Sie möchten mir einen Kaffee spendieren?
Anmerkungen oder sonstige Ideen und Vorschläge können Sie gern per Mail an info@lernzettel.org bzw. fehler@lernzettel.org senden.